CAP、CLIA、ISO15189分别是什么认证?
时间:2023-08-17 08:42:44 访问量:468临床检验实验室的核心是为临床提供高质量的检验报告。市场上临床检测实验室林立繁多,各个实验室如何才能向外界证明实验室管理能力和质量水平呢?许多实验室会选择参加行业内具有影响力的实验室资质认证和室间质评,常见的有CLIA、CAP、ISO15189等,来展示其质量管理体系及技术水平。
CLIA认证
CLIA(Clinical Laboratory Improvement Amendments),即临床检验改进修正计划,于1988年被美国国会通过,由医疗保险和医疗补助服务中心(Center for Medicare & Medicaid Services,CMS)颁布,用于规范实验室的质量管理体系。
在美国,CMS要求所有的临床实验室必须通过CLIA的认证注册,才有权接收并处理血液、体液和组织等人体样本,以用于疾病的诊断、预防、评估和治疗,其提供的检测服务才能向美国政府的医疗保险和医疗补助计划收费。多个癌种的NCCN指南中也对生物标识物的检测机构提出了明确要求:进行生物标志物的检测需在具有CLIA认证的实验室中进行。

CLIA实验室主要由三个机构监管,分别是医疗保险和医疗补助服务中心(CMS)、疾病控制和预防中心(CDC)、美国食品和药物管理局(FDA)。

值得注意的是,CMS的审计政策包括:预先通知的初审,两年一次的定期重审,以及事先不通知的处理投诉的突击审计。CLIA的目标是确保临床检验实验室的数据质量符合要求,它更加关注结果,而非过程,其审计程序是结果导向的,鼓励教育式审计。
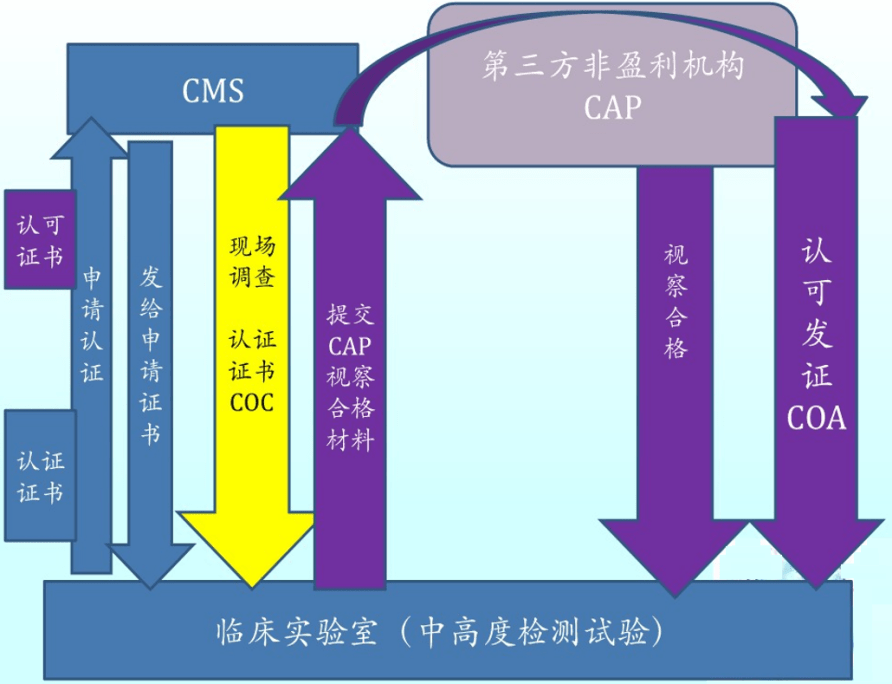
CLIA的证书分为三种(COC、COA、COR证书),均为2年效期。
a、COC:certificate of compliance
b、COA:certificate of accreditation
c、COR:certificate of register
通过CLIA认证有多重意义,除了能够证明实验室自身的技术管理水平,表明实验室出具结果报告的准确性、可靠性和时效性之外,还能够拓展海外业务,进入美国市场,为美国患者提供临床检验的资质,同时还具备了参与要求执行CLIA标准的全球临床试验的资格。
CAP认证
CAP(College of American Pathologists,美国病理医师协会)是被CLIA法案批准认证的认证机构之一,成立于1947年,是目前世界上最大的病理学家组织,专由临床检验学家和病理学家组成。
CAP认证涵盖包括临床遗传学检测在内的所有实验室专业,根据CLIA要求,对临床实验室各个学科全方面制定详细的检查单并严格要求,来确保实验室符合质量标准,从而改进实验室的实际工作,确保病人检测结果的准确性。

在正式申请CAP认证之前,实验室必须要有满足申请标准要求的实验室主任,要参与实验室能力测试(proficiency testing,PT),并能进行患者相关项目的检测。
已获得CAP认证的实验室也将被强制要求参加所有认证项目相关的CAP-PT能力测试,并经历每两年一次的重新审核,以为了确保实验室的质量管理持续受到持续监管。
CLIA与CAP的区别与联系
CLIA是强制执行,所有美国的临床检验实验室都必须执行。CAP是可选项,是独立的实验室认证体系。申请二者的难易程度不同。
CLIA是核心条款,CAP既包括全部CLIA条款,又在细节上进行了丰富,二者详略不同。
CAP可以取代CLIA的两年一次的重审,但是不能取代CLIA的初审。
CAP与CLIA对比国内来看,CLIA相当于基础的“医疗执业机构许可”的申请,CAP是相当于ISO15189认可。前者偏政府行为,后者为公正的三方行为。
CLIA认证最独特之处在于:即使未获FDA批准,实验室LDT项目也完全可在其实验室范围内提供分子检测业务,以指导临床。当然,如果外售还须经过FDA批准。而仅获得CAP认证的实验室,如果产品未获FDA批准,则完全不能临床应用。
CAP、CLIA,认证哪一个?
在临床检测行业内,CAP与CLIA双认证被视为国际最高水平的认证标准,在全球范围内均受认可。相比于CAP,获得CLIA认证的难度更大,但相同的是,CLIA每两年也需进行重新评审。
预算允许的情况下,可以选择AII IN。不过目前,国内同时获得CLIA和CAP认证的企业屈指可数。
国内企业从市场角度,多数选择首先拿到CAP证书,足以开展相关竞争工作。企业如有海外业务需求,或合作海外企业要求提供CLIA证书,则再增加CLIA认证。在CAP满足的基础上,CLIA可谓是锦上添花的工作。
ISO15189 / CNAS-CL02
ISO(International Organization for Standardization即国际标准化组织)是全球最大最权威的标准化组织,涵盖了上百个国家的成员国,在各个领域制定和颁布国际标准上万余条。
ISO15189即《医学实验室-质量和能力的要求》,由国际标准化组织(ISO)在2003年2月15日正式颁布,分别在2007年、2012、2022年进行了改版,目前使用版本为ISO15189:2022。
IS015189由各国相应组织颁发证书,比如我国的CNAS。
目前,我国对医学实验室进行ISO15189认可的唯一权威机构是中国合格评定国家认可委员会(CNAS),CNAS将ISO15189:2022直译成中文,重新命名为CNAS-CL02:2023《医学实验室质量和能力认可准则》。
获得ISO15189认可的重要意义:
表明具备按相应认可准则开展检测服务的技术能力。ISO15189受官方机构认可,医学实验室获得该认证证明其出具的检测报告准确有效,获得客户信任。
提高医学实验室质量和能力,以及人员素质。医学实验室按照ISO15189的要求,搭建质量管理体系,培训考核实验人员,可大大提高实验室人员的专业技能,完善工作流程,提高工作效率,提升实验室能力水平。
增强社会知名度及市场竞争力。ISO15189既然是国际标准,通过其认可也间接证明了实验室管理水平达到了国际标准,赢得政府部门、社会各界的信任。
避免医疗纠纷。实验室根据ISO15189要求,建立一套完善、规范的质量体系,实验人员严格按程序文件进行标准化操作,对所有记录以及实验数据进行有效管理。确保在病人提出质疑或索赔时,做到有据可依。
与国际接轨,促进国际贸易。通过与国际组织、区域组织或国外认可机构签署多边或双边互认协议,促进实验室检测结果的国际互认,从而促进对外贸易。

版权所有 © 2008-2017 北京智臻管理咨询有限公司 技术支持:展为网络
Top

